ASSISTANCE MÉDICALE À LA PROCRÉATION
Notre équipe multidisciplinaire de professionnels expérimentés s’engage à fournir des soins personnalisés et innovants pour vous aider à réaliser votre rêve de fonder une famille. Nous sommes dévoués à vous accompagner tout au long de votre parcours vers la parentalité.
- Fécondation naturelle
- La stimulation simple de l’ovulation
- Insémination intra-utérine
- Fécondation In Vitro
- Prélèvement chirurgical de spermatozoïdes
- Accueil d’embryons
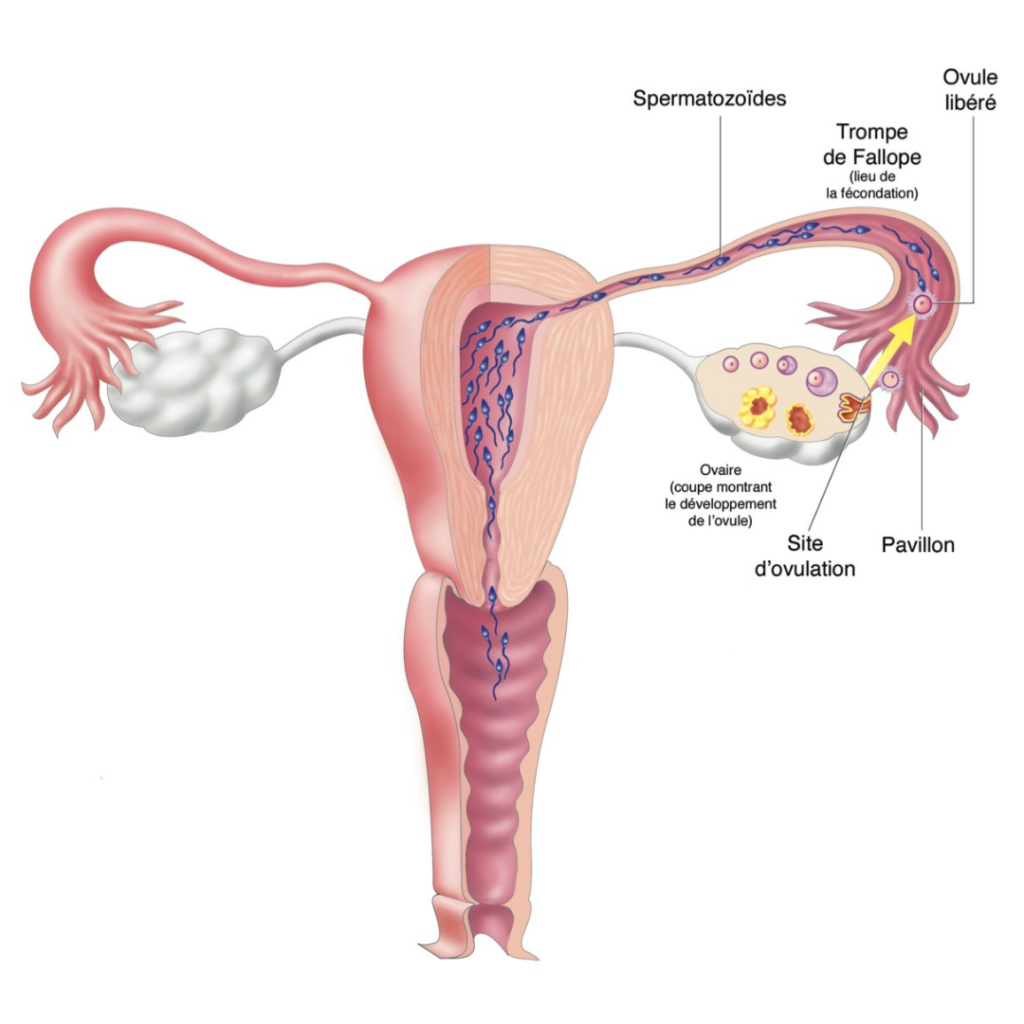
Elle est issue de la rencontre dans la trompe de deux gamètes : L’ovocyte de la femme et le spermatozoïde de l’homme.
La fécondation permet la création d’un embryon qui migrera de la trompe vers la cavité de la paroi utérine, où il s’implantera.
A chaque cycle chez la femme, un seul follicule dans l’ovaire est sélectionné et se développe sous l’action d’hormones produites par l’hypophyse (glande à la base du cerveau).
Le follicule grossit progressivement pour atteindre sa maturité jusqu’à atteindre une taille de 20 mm.
Il contient un ovocyte qui est baigné dans le liquide intrafolliculaire et qui, lorsque le follicule est mature, est libéré sous l’effet d’hormones et se retrouve dans la trompe où il attend les spermatozoïdes.
Cet ovocyte est de très petite taille par rapport à la taille du follicule (0,15 mm de diamètre).
Après un rapport sexuel, plusieurs millions de spermatozoïdes sont déposés au fond du vagin , seules quelques millions montent rejoindre l’ovocyte dans la trompe où seul un spermatozoïde ( L’ELU) pénètre dans l’ovocyte.
La fusion des 2 noyaux donne naissance à l’embryon qui migre sur 5 jours dans la cavité utérine pour s’y enfouir : c’est la nidation ou implantation.
La fertilité naturelle dans l’espèce humaine n’est pas de 100 % mais de 20 à 25 % par cycle.
Elle diminue avec l’âge chez la femme et de façon moindre chez l’homme.
Certaines patientes n’ont pas d’ovulation et il est possible de leur proposer une induction de l’ovulation simple afin d’obtenir la croissance d’un follicule et permettre de les aider à obtenir la grossesse.
Cette induction de l’ovulation peut faire appel à trois types de thérapeutiques.
- Le citrate de clomiphène
Sous forme de comprimés à prendre pendant 5 jours à partir du 2ème ou 3 ème jour du cycle et qui n’est utilisé que chez les femmes présentant un trouble de l’ovulation isolé.
Il n’est pas employé si une technique de PMA (insémination ou FIV) est envisagée.
Dès qu’un follicule est mature, une injection sous cutanée d’une hormone hCG , est prescrite afin de déclencher l’ovulation.
- Les gonadotrophines
Ce traitement est administré quotidiennement par voie sous cutanée au niveau du ventre ou de la cuisse afin de stimuler la croissance folliculaire.
Ces injections contiennent de la FSH seule ou de la FSH + LH selon les indications.
L’ovulation , déclenchée par l’hCG, survient 36 à 48 heures après l’injection.
- La pompe à GnRH
Il s’agit d’un petit dispositif relié à un fin cathéter souple placé en sous cutané et laissé pendant plusieurs jours.
C’est un réservoir qui contient une hormone de synthèse appelée GnRH et contrôlé par une télécommande qui permet au produit d’être délivré de façon régulière.
Ce traitement n’est pas utilisé en FIV et s’adresse à des cas rares de troubles de l’ovulation secondaire à une anomalie de sécrétion des hormones de la commande centrale situé à la base du cerveau.
Une insémination intra-utérine est une technique simple.
Une stimulation de l’ovulation est prescrite, la plupart du temps par voie injectable de façon à optimiser la croissance des follicules et de l’endomètre.
L’ovulation est repérée grâce à un monitorage de l’ovulation qui consiste à pratiquer une échographie et une prise de sang environ 5 à 7 jours après le début du traitement.
Quand le follicule est mature, on déclenche l’ovulation par une injection d’HCG (OVITRELLE) qui libèrera le follicule 36 à 40 heures plus tard.
Le conjoint fait alors un recueil de sperme au laboratoire d’aide médicale à la procréation, situé au rez-de-chaussée de la maternité.
Le sperme est préparé par une technique de lavage et centrifugation et vous récupérez la préparation obtenue 2 heures après le recueil.
Une abstinence de 2 à 4 jours maximum est recommandée avant l’insémination.
L’insémination est réalisée au cabinet du gynécologue référent environ 2 heures plus tard.
Il s’agit d ‘un geste indolore pratiqué à l’aide d’un petit cathéter pour déposer les spermatozoïdes dans la cavité utérine.
Un repos n’est pas nécessaire et vous pouvez vaquer à vos activités sans précaution particulière après le geste.
Un traitement par progestérone est la plupart du temps prescrit après l’insémination et un test de grossesse peut être pratiqué 12 à 14 jours après l’insémination.
En général, nous n’allons pas au-delà de 4 inséminations si une grossesse n’est pas obtenue.
La FIV est proposée dans les situations où le processus naturel de fécondation n’arrive pas à se produire.
Les ovocytes sont prélevés au niveau de l’ovaire par ponction puis mis en contact avec les spermatozoïdes au laboratoire de biologie de la reproduction.
L’embryon obtenu sera ensuite déposé à l’intérieur de l’utérus pour s’y implanter.
La stimulation ovarienne est plus importante afin de recueillir plusieurs ovocytes.
Au laboratoire , 2 techniques sont utilisées :
- La FIV conventionnelle ( classique) qui s’adresse principalement aux infertilités féminines ( problème de perméabilité tubaire, endométriose), aux infertilités masculines peu sévères et aux infertilités inexpliquées souvent après échec des IIU.
- La FIV par injection intracytoplasmique d’un spermatozoïde (ICSI) est proposée principalement en cas d’infertilité masculine sévère ou en cas d’absence d’embryon lors d’une FIV Conventionnelle faite antérieurement. Un spermatozoïde est injecté au moyen d’une micro-pipette dans chaque ovocyte. L’IMSI est une technique identique à l’ICSI sauf que le choix du spermatozoïde est fait à l’aide d’un microscope plus puissant.
Après réalisation de la FIV au laboratoire, on obtient des embryons.
Dans la majorité des cas l’embryon est ensuite transféré au stade «blastocystes» qui est le stade embryonnaire obtenu après 5 à 6 jours de culture dite «prolongée» au laboratoire.
C’est à ce stade physiologiquement que l’embryon s’implante dans la cavité utérine.
Les avantages du transfert à ce stade sont une meilleure sélection embryonnaire, un transfert plus physiologique par une meilleure synchronisation utérus/embryon.
Toutefois , les embryons obtenus à J 2 ou J 3 post ponction n’atteignent pas tous le stade de blastocystes ce qui entraine un taux réduit d’embryon.
L’absence de blastocystes est consécutive à un arrêt de développement in vitro des embryons placés en culture prolongée.
Dans certaines situations, il est parfois proposé le transfert à J 2 ou J 3 post ponction.
Il est parfois nécessaire de procéder à un prélèvement chirurgical des spermatozoïdes en cas d’azoospermie (absence de spermatozoïde dans le sperme après éjaculation) après avoir réalisé les examens nécessaires (dosage hormonaux, échographie génitale…).
En cas d’obstacle sur les voies excrétrices par lesquelles passe l’éjaculat, il conviendra d’aller prélever les spermatozoïdes dans le canal à proximité d’un testicule : le canal epididymaire.
En cas d’absence d’obstacle sur les voies excrétrices, soit les spermatozoïdes produits par les testicules ne peuvent en sortir, soit la production est si faible qu’on ne retrouve pas de spermatozoïdes dans l’éjaculat. On procédera donc au prélèvement d’une pulpe testiculaire qui sera ensuite disséquée au laboratoire pour évaluer ou non la présence de spermatozoïdes : c’est la biopsie testiculaire.
Cette intervention nécessite une hospitalisation très courte et est réalisée sous anesthésie générale par un urologue spécialisé en andrologie.
Les spermatozoïdes retrouvés sont ensuite congelés en attendant la réalisation de la FIV ICSI.
L’accueil d’embryons est une technique d’AMP soumise à autorisation. Sur le Nord-Pas de Calais, seul le CHU de LILLE est autorisé pour cette activité, nous travaillons en concertation avec l’équipe clinico-biologique d’AMP du CHU pour mener à bien ces demandes.
Au décours d’une FIV, seuls 1 à 2 embryons sont transférés pour limiter le risque de grossesse multiple. Les embryons restants, surnuméraires, s’ils sont de qualité suffisante, peuvent être congelés si c’est votre souhait. Si votre projet parental est réalisé, avec le nombre d’enfants souhaités, et qu’il vous reste des embryons congelés, vous êtes interrogés annuellement sur votre souhait vis-à-vis de ces embryons. Vous pouvez ainsi choisir d’en faire don pour aider d’autres couples à réaliser leur projet parental.
Si vous choisissez cette option, nous reverrons votre dossier afin d’établir si, au regard des éléments médicaux connus à l’époque de votre tentative de FIV, du nombre et de la qualité embryonnaire, il semble possible d’accéder à votre souhait. Nous vous enverrons des questionnaires. À réception de ceux-ci, une partie de votre dossier sera communiquée à l’équipe clinico-biologique du CHU de LILLE. C’est ensuite l’équipe du CHU qui reprendra contact avec vous pour poursuivre la démarche.
Les couples demandeurs de ce don d’embryons, sont :
- Des couples nécessitant le recours à un double don (spermatozoïdes et ovocytes).
- Des couples infertiles pour lesquels les tentatives d’AMP sont impossibles.
- Dans de rares cas, certains couples pour lesquels les tentatives d’AMP ont échoué.
Dans tous les cas, couples « donneurs » et « receveurs » ne se connaissent pas, le don restant anonyme en France, et il n’y a aucune contrepartie financière.
Risques et Complications
Chez nous, la transparence et l’information sont des valeurs fondamentales, et nous croyons qu’une compréhension approfondie des risques potentiels est essentielle pour chaque patient.

Risques liés aux traitements
L’hyperstimulation
Dans certains cas, la réponse des ovaires aux traitements de stimulation est excessive. Il y a alors le risque que survienne, après le déclenchement de l’ovulation, une réaction d’hyperstimulation des ovaires.
Celle-ci se caractérise par une augmentation du volume des ovaires qui deviennent très douloureux.
Dans certains cas, s’y associe un épanchement liquidien dans le ventre voire dans la plèvre.
Dans les cas sévères, une phlébite ou une embolie pulmonaire.
Une hyperstimulation sévère nécessite alors une hospitalisation pour rééquilibration hydro-électrolytique, et surveillance. En fait, certaines femmes sont plus à risque que d’autres (aspects échographiques évocateurs, bilan hormonal initial) et nous adaptons préventivement les traitements de stimulation. Il faut savoir que cette complication ne diminue pas les chances de grossesse.
Certaines femmes présentent un terrain favorisant les thromboses veineuses (phlébite…)
Chez ces femmes, le risque est accru lors des traitements de stimulation, et a fortiori en cas de grossesses. Ceci peut avoir des conséquences graves. C’est pourquoi, il est capital de nous signaler tout antécédent personnel ou familial, de phlébite ou embolie pulmonaire.
Un bilan plus approfondi est alors réalisé, préalablement à la FIV et un traitement anti-coagulant préventif est mis en place si nécessaire.
Risques liés à la ponction
- Anesthésie
Toute anesthésie, qu’elle soit générale ou locale, comporte un risque exceptionnel. La consultation préanesthésique et la surveillance après l’intervention ont pour but de réduire au minimum ces accidents, qui ne sont pas propres à la fécondation in vitro et qui restent exceptionnels.
- Infection
Il peut s’agir du réveil d’une infection génitale préexistante et latente ou d’une conséquence directe de la ponction. Cet accident est rare (moins de 1/500 environ) mais nécessite que vous nous recontactiez en cas de douleurs associées à de la fièvre après la ponction.
Un traitement antibiotique est prescrit avant la ponction, en cas de situation à risque.
- Hémorragies intra-abdominales
C’est un accident très rare (environ 1/1000) mais qui justifie que vous restiez quelques heures en observation après la ponction même si celle-ci s’est bien déroulée.
Au total, les complications des ponctions échoguidées trans-vaginales sont réelles mais exceptionnelles.
Grossesse extra-utérine
Alors que la GEU survient dans 1 à 1,5% des conceptions naturelles, sa fréquence est d’environ 2% en cas de FIV.
Grossesse multiple
Afin de limiter les risques des grossesses multiples, la règle est de ne transférer qu’un ou deux embryons, en fonction de l’âge de la patiente, du nombre et de la qualité embryonnaire.
Risque éventuel de cancer
Depuis le début de la FIV et de l’utilisation des traitements de stimulation, la question récurrente de l’impact de ces traitements sur le développement de cancers du sein, des ovaires et de l’utérus se pose.
On peut aujourd’hui dire que l’ensemble des études est rassurant : aucun lien entre ces cancers hormono-dépendants et les traitements inducteurs de l’ovulation n’a pu être prouvé.
Il convient de rester prudent, car le suivi de ces patientes a été fait sur un temps relativement court, alors que ces cancers apparaissent pour la plupart plus tardivement. Ces données sont donc régulièrement réévaluées.
Au-delà de ces traitements en vue d’AMP, il conviendra que vous soyez suivie comme toutes les femmes avec un examen gynécologique régulier, associé à une mammographie et éventuellement une échographie pelvienne.
Difficultés psychologiques
Un traitement par FIV comporte des contraintes importantes et consomme beaucoup de temps et d’énergie. C’est un long parcours demandant beaucoup d’investissement de soi et du couple.
Si le traitement par FIV suscite de grands espoirs, la réussite n’est pas toujours au rendez-vous puisqu’environ 1 couple sur 4 obtient l’enfant désiré après un essai.
Cette déception peut induire un sentiment de dévalorisation et d’injustice. Dans certains cas, une réaction dépressive peut apparaître.
Une aide psychologique spécialisée est parfois souhaitable et bénéfique. Elle permet de s’exprimer, faire le point et relativiser ce qui se passe auprès d’une personne « neutre » mais très au fait de ces problèmes. Si vous en éprouvez le besoin, vous pouvez en parler à votre gynécologue qui vous adressera au Dr Charlotte BUTEZ, pédopsychiatre spécialisée en périnatalité ou au Dr Nathalie BLAIRE, psychiatre qui exercent au sein de l’Hôpital privé Le Bois.
Risque pour l'enfant né après FIV
- Les malformations
Dans la population générale le taux de malformations observées à la naissance est de 2.5%.
Après FIV, le taux de malformations observé est de 3%. Ce taux est le même, en cas de grossesse survenue spontanément chez les couples hypofertiles.
Ces données laissent à penser que la légère augmentation des malformations observées serait liée au terrain de l’infertilité, et non pas à la technique d’AMP.
Il est admis que certaines anomalies très rares (touchant environ 1 nouveau-né sur 15000) deviennent plus fréquentes après FIV (touchant alors environ 1 nouveau-né sur 4000).
En cas de problème spermatique :
Le risque de transmettre un problème de stérilité masculine, hérité du père, à un garçon ne peut pas être correctement évalué à ce jour mais il est probable dans certains cas.
On ne sait, à l’heure actuelle, diagnostiquer que très peu des nombreuses causes génétiques pouvant être responsables de l’infertilité masculine. Certaines de ces anomalies sont associées à des maladies rares ne s’exprimant qu’au fil de l’âge. On peut se demander si rendre fécondants de tels spermatozoïdes ne contribuera pas à l’apparition ultérieure de ces maladies, même s’il est probable selon les données acquises que ceci ne se fera que dans une faible proportion des cas.
- Les anomalies chromosomiques
Dans la population générale le taux d’anomalies chromosomiques observées à la naissance est de 0.9%.
L’incidence des anomalies chromosomiques est augmentée après ICSI : 1,6% d’anomalies non héritées (caryotype normal du père).
Ces anomalies chromosomiques sont de gravité très variable : si certaines conduisent à une interruption thérapeutique de la grossesse, d’autres sont tout à fait compatibles avec une vie normale et ne seraient détectables qu’en cas d’analyse des chromosomes (caryotype).
Une consultation de conseil génétique est systématiquement proposée en cas d’anomalie du caryotype d’un des deux conjoints et est aussi accessible à ceux qui souhaitent une information supplémentaire.


- 110 Av. de Dunkerque, 59000 Lille
- 03 20 92 98 04
- secretariat@amp-hplb-lille.com




